肺大細胞神經內分泌癌(L-LCNEC)是肺癌的一個亞型,其發病率低,惡性程度高。對於早期患者,手術治療受限,且術後復發的風險高。對於無法切除或晚期的患者,以鉑類為基礎的化療是目前的主要治療方法,但其療效並不令人滿意。帶有間變性淋巴瘤激酶(ALK)基因突變的L-LCNEC非常罕見,目前沒有標準療法。在這篇文章中,我們報告了一個攜帶ALK基因突變的局部晚期L-LCNEC的患者 ,接受阿來替尼一線治療。該患者為一名既往健康的46歲非吸煙女性,被臨床診斷為患有不可切除的局部晚期L-LCNEC。患者血漿和腫瘤標本的下一代測序(NGS)顯示棘皮動物微管相關蛋白樣4(EML-4)(外顯子13)-ALK(外顯子20)融合,突變丰度分別為14.48%和15.37%。患者拒絕化療,並接受了阿來替尼一線治療,服用劑量 600mg,一日兩次。在服用阿來替尼1個月後,患者的胸部增強計算機斷層掃描(CT)顯示出部分緩解(PR)。在使用阿來替尼治療12個月後,影像學評估顯示,患者保持了PR。治療開始時觀察到患者有2-3級的皮疹。經過對症治療後,皮疹消失,且副作用完全耐受。目前,患者可以正常工作,功能狀態為0,未發生任何重大不良事件。病例表明,對具有基因突變III期的L-LCNEC患者在一線使用靶向治療也是一個不錯的選擇。其副作用輕,患者耐受性好,並可提高生活質量。
背 景
肺大細胞神經內分泌癌(L-LCNEC)是神經內分泌腫瘤(NET)的一種類型。它是一種罕見的、低分化且高度惡性的肺部腫瘤。它在所有肺部惡性腫瘤中的占比<3%。L-LCNEC被定義為一種非小細胞肺癌(NSCLC)。它具有侵襲、廣泛轉移和存活率低的特點。其臨床特徵和預後與小細胞肺癌(SCLC)相似。由於其非常罕見,目前對其診斷、治療和預後仍存在諸多爭議,相關治療和預後指標缺乏大樣本研究和文獻數據支持。
大量的基因突變已被證明可以驅動一系列人類癌症類型的惡性轉化和細胞增殖,包括肺癌。間變性淋巴瘤激酶 (ALK)基因重排發生在~5%的肺癌中,是靶向治療的一個生物標誌物。迄今為止,包括阿來替尼在內的幾種ALK抑制劑已經被開發出來,並作為對鉑類雙藥化療耐藥的患者的替代或一線選擇。基因組異常最常見於L-LCNEC中,其次是類癌和SCLC。然而,由於L-LCNEC的發病率較低,其分子特徵和治療意義仍不清楚。到目前為止,只有少數攜帶ALK重排的L-LCNEC患者相關病例報道;然而,這些患者的治療方法各不相同、 很少有患者接受過酪氨酸激酶抑制劑一線治療。
本文報告了一例攜帶ALK突變的局部晚期L-LCNEC患者的病例,該患者接受了一線阿來替尼靶向治療,顯示出良好的療效。
病 例
2020年11月18日,一名既往健康的46歲非吸煙女性因感冒後咳嗽和排痰到深圳市南山區蛇口人民醫院就診。胸部計算機斷層掃描(CT)顯示右葉有一個結節(無具體報告)。醫院的醫生建議住院進一步診斷和治療,但患者很害怕並拒絕。隨後,她用傳統的中醫藥進行治療。2021年6月13日,她因同樣的原因到同一醫院就診,再次進行胸部CT檢查發現,與2020年11月18日的CT相比 ,右肺上葉的病變比以前更多,縱隔淋巴結明顯增大,很可能是周圍型肺癌。
該患者於2021年6月16日住院治療。在 2021年6月17日,胸部CT顯示右肺上葉前段有一個19×16×30mm的結節狀陰影,鄰近胸膜受累,並在右側肺門和縱隔的2R和4R / L(右/左)處觀察到多個腫大的淋巴結。較大淋巴結的短直徑約為21mm。上腔靜脈腔因淋巴結推擠而變窄,並考慮淋巴結轉移(圖1)。2021年6月21日,進行了超聲支氣管鏡檢查,在縱膈的4R、4L和縱膈的7個區域、右肺門(10R)和右小葉間(11R)發現多個低回聲腫塊。病變的最大短直徑約為20.4×30.6mm,在4R區(圖2)。
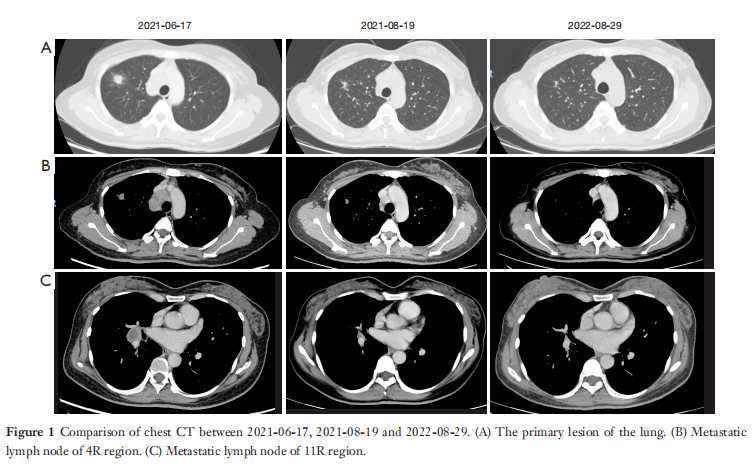
圖1 2021-06-17、2021-08-19和2022-08-29的胸部CT對比。(A)肺部的原發病變。(B)4R區的轉移性淋巴結。(C) 11R區的轉移性淋巴結。
圖2 超聲支氣管鏡 (A)是4R區域的轉移淋巴結(最大的淋巴結短直徑為20.4×30.6mm)。(B) 是 11R區域的轉移性淋巴結(最大的淋巴結短直徑為12.9×21.6mm);在其中可以看到血流信號。
在超聲引導下,用21g活檢針在縱隔11R區和4R區進行經纖維支氣管針吸活檢術。2021年6月22日,病理結果顯示11R和4R淋巴結低分化癌,結合免疫表型,符合神經內分泌癌,傾向於L-LCNEC。
免疫組織化學(IHC)結果:甲狀腺轉錄因子1(TTF-1)、細胞角蛋白-7(CK7)、AE1/AE3、神經細胞黏附分子(NCAM、CD56)、嗜鉻粒蛋白A(ChrA)、突觸素(Syn)陽性,以及Ki-67陽性率為40%,但NapsinA、P40和P63為陰性(圖3)。臨床分期為cT1cN3M0 IIIB。對患者的血漿和腫瘤標本進行了NGS多基因檢測,顯示棘皮微管相關蛋白樣4(EML-4)(外顯子13)-ALK(外顯子20)融合,突變丰度分別為14.48%和15.37%,微衛星穩定(MSS),腫瘤比例評分(TPS)0%,綜合陽性得分(CPS)1。
圖3 縱隔淋巴結穿刺術的病理結果 (A) 組織學10×HE。
(B)B組織學40×HE。 (C) 腫瘤表達Syn 20×HE。(D) 腫瘤表達CgA 20×HE。HE,蘇木精和伊紅。
經過胸部腫瘤外科醫生的評估,醫生建議術前進行2-4個周期的新輔助化療,並進行綜合評估以確定是否可以進行手術切除。患者因個人原因拒絕化療,2021年7月18日,根據中國臨床腫瘤學會(CSCO)2020年指南,患者開始使用ALK酪氨酸激酶抑制劑阿來替尼治療,劑量為600 mg,每日兩次。經阿來替尼治療1個月後,肺腫瘤大小由19×16×30縮小至13×11×14 mm,最大肺門及縱隔淋巴結由21 mm縮小至14 mm,上腔靜脈壓力也有所下降(圖1)。根據實體瘤療效評估標準(RECIST1.1),該腫瘤反應判定為部分緩解(PR)。隨後,患者每2個月接受一次檢查,腫瘤繼續縮小。2022年6月24日,患者做了正電子發射斷層掃描(PET)-CT,仍有腫瘤殘留,腫瘤大小與2022年4月28日相同。2022年8月29日,也就是阿來替尼治療12個月後,肺部腫瘤大小已縮小到9×6 mm(與2022年4月28日胸部CT相比),肺門和縱隔淋巴結短直徑為8 mm,癌胚抗原(CEA)水平繼續下降(圖4)。
圖4 腫瘤標誌物CEA逐漸降低。CEA,癌胚抗原。
與治療相關的不良事件包括皮疹,在服藥半個月後觀察到皮疹出現在病人的手、腳和四肢上。根據NCI-CTCAE5.0標準,皮疹為2~3級。患者接受了抗過敏藥物氯雷他定片、皮膚護理、內服外用中藥等對症治療,1個月後皮膚開始剝離。在2021年8月複查時,患者的皮疹已基本消失,雖然部分皮膚仍有色素(圖5),但經過6個月的藥物治療,皮膚顏色已基本恢復正常。總體耐受性可接受,未觀察到其他不良反應,患者能夠正常生活和工作。病例的時間表如(圖6)所示。
圖5 治療相關的不良皮疹。(A)手掌上出現皮疹。(B、C)對症治療後,皮膚逐漸剝離,然後恢復正常。(D)手背出現皮疹。(E)對症治療後皮疹消退,無色素沉著。(F)上肢出現皮疹。(G)在服藥過程中,皮疹消退,但在對症治療後仍有色素沉著。
圖6 病例時間表。CT,計算機斷層掃描;NGS,下一代測序;L-LCNEC,肺大細胞神經內分泌癌;NGS,下一代測序;EML4,棘皮微管相關蛋白樣蛋白4;ALK,間變性淋巴瘤激酶
討 論
L-LCNEC是一種罕見的高侵襲性肺癌,屬於非小細胞肺癌的一種。Travis等人首次將其確定為肺癌的一種新亞型。2011年,世界衛生組織將L-LCNEC列為大細胞癌。在2015年與小細胞肺癌、典型類癌、不典型類癌一起被重新歸類為肺部NET。大約20%的L-LCNEC有與SCLC或NSCLC混合的腫瘤成分。為了研究L-LCNEC與SCLC和NSCLC之間的生物學關係,Rekhtman等人分析了L-LCNEC和其他主要肺癌類型的基因組變化。發現L-LCNEC主要包括以下兩個不同的亞群,具有不同的基因組特徵:SCLC樣亞型(特點是TP53+RB1共突變/缺失和其他SCLC類型改變);NSCLC樣亞型(特點是缺乏TP53+RB1共變,幾乎普遍出現STK11、KRAS和KEAP1的NSCLC型突變)。
已有研究確定L-LCNEC的生物學行為和預後。一些人認為L-LCNEC具有神經內分泌特徵,應該被認為是小細胞癌。到目前為止,還沒有隨機對照試驗來檢驗L-LCNEC的最佳治療方案。Derks等人進行了一項回顧性研究,發現L-LCNEC是一種像小細胞肺癌一樣有高度侵襲性的肺癌,在疾病的所有階段預後都很差。然而,L-LCNEC和SCLC之間有重要的區別。值得注意的是,在IV期,L-LCNEC患者的預後比SCLC患者更差,然而,目前用於治療早期L-LCNEC的治療方法與用於治療SCLC的方法不同。有研究表明,晚期L-LCNEC治療方案,用小細胞肺癌的鉑類化療方案客觀緩解率(37-52%)高於非小細胞肺癌鉑類化療方案(12-50%)。然而,患者的反應通常是短暫的,中位無進展生存(PFS)時間為4.6-6.1個月,中位總生存(OS)時間較差為10.2-11.1個月。另一項研究顯示,接受化療的IIIB和IV期L-CNEC患者預後不良,中位PFS時間為5.2個月,OS時間為5.2個月。
L-LCNEC IHC的主要特徵是表達神經內分泌相關標記物,如CD56、CgA和Syn,可作為NSCLC病理鑑別診斷的標誌物。在本文中,我們報告了一個罕見的病例,患者被診斷為神經內分泌癌,很可能是大細胞神經內分泌癌。免疫組化檢測的結果是,如CD56、 ChrA和Syno等神經內分泌標誌物均為陽性。
酪氨酸激酶的基因突變在肺腺癌的發病機制中起著重要作用。攜帶ALK重排的腫瘤可以用ALK抑制劑成功治療。ALK重排在肺腺癌中最為常見。
攜帶ALK重排的L-LCNEC非常罕見,目前還沒有針對這種疾病進行大規模的臨床試驗。然而,報道稱ALK陽性的腫瘤通常表達TTF-1。本例患者為TTF-1陽性(3+),但經與本院病理科溝通,確診患者為單純性L-LCNEC。此外,在患者的基因檢測結果中沒有檢測到TP53+RB1共突變,推測患者患有一種類似NSCLC樣亞型。
目前,腫瘤的治療模式比幾十年更加個性化和精準化。CSCO和國家綜合癌症網絡發布的NSCLC指南均建議患者接受多基因檢測,以明確分子分型。本文患者進行了NGS檢測,檢出EML4-ALK(E13:A20)重排(融合),這是最常見的重排(融合)位點。近年來,已有多個病例報道L-LCNEC存在ALK重排。事實上,最早的兩例L-LCNEC報告就報告了ALK重排。第一個案例涉及到一名43歲的女性,她從未吸煙,並在一線接受了克唑替尼的靶向治療。經過6周的治療,出現腦轉移和皮膚轉移,這表明腫瘤對克唑替尼具有耐藥性。第二個病例是一名60歲的女性,她從不吸煙,也沒有接受任何ALK抑制劑。此外,Hayashi等人報告了一例75歲、不吸煙的女性,被診斷為L-LCNEC合併多發性肝臟和骨轉移。經過7個周期的細胞毒性藥物化療後,基因檢測顯示ALK重排。隨後服用了阿來替尼。約1個月後,腫瘤標誌物神經元特異性烯醇化酶(NSE)和胃泌素釋放肽前體(ProGRP)降至正常範圍,4個月後,肺部病變由21 mm縮小至16 mm,肝臟病變消退,患者達到PR。經過6個月的治療,正電子發射斷層掃描-CT顯示病情穩定。本病例中患者處於cT1cN3M0 IIIB臨床分期階段,當時尚無手術指征。這名患者因個人原因拒絕化療,並要求進行靶向治療。
根據ALESIA中III期臨床研究結果。2018年,中國國家藥品監督管理局批准阿來替尼用於治療ALK陽性的局部晚期或轉移性非小細胞肺癌,包括作為一線治療藥物或克唑替尼治療進展後的二線藥物。由於阿來替尼一線治療的中位PFS時間為34.8個月,CSCO指南建議將其作為ALK陽性患者的一線治療。
在本病例中,經過阿來替尼1個月的靶向治療後,腫瘤顯著縮小,患者實現了PR。然後每兩個月定期檢查一次腫瘤,並繼續縮小。治療1年後,對腫瘤進行複查,維持PR狀態。治療初期出現2~3級皮疹,治療後皮疹迅速好轉,未再出現。未觀察到其他不良反應,患者能夠正常生活和工作。
先前的研究表明,對於晚期L-LCNEC,姑息化療對於SCLC比NSCLC更適用。免疫治療也被嘗試用於治療L-LCNEC。對於適合進行靶向治療的患者,一線靶向治療也是一個不錯的選擇,未來還需要更多的試驗和研究,以探索L-LCNEC的最佳和合適的治療方法。在這種情況下,遺憾的是最初沒有為患者進行ALK免疫組化檢測,我們將在以後改進相關的免疫組化檢測。
對於具有不能切除的III期和0-1級功能狀態的NSCLC患者,建議進行多學科小組討論,根據2020年CSCO指南的一級推薦,根治性同步放化療或度伐利尤單抗作為同期放化療後的鞏固治療。對於IV期驅動基因陽性的非小細胞肺癌患者首選靶向治療。但對於拒絕化療並有基因突變的III期患者來說,靶向治療也是一個很好的選擇,上述病例中,患者選擇了靶向治療,拒絕了化療和手術,她取得了良好的療效,沒有明顯的嚴重副作用,提高了生活質量。
參考文獻:Chen D, Ma S, Sun L, Lang Y, Yang B. EML4-ALK rearrangement of lung large cell neuroendocrine carcinoma: a case report. Ann Transl Med. 2023 Jan 31;11(2):134. doi: 10.21037/atm-22-6062. Epub 2023 Jan 11. PMID: 36819595; PMCID: PMC9929752.