近日,國家藥監局發布通告指出
經江蘇省食品藥品監督檢驗研究院等
11家藥品檢驗機構檢驗
共17家企業生產的
19批次藥品不符合規定
詳情如下
國家藥監局關於19批次藥品
不符合規定的通告
(2024年第47號)
經江蘇省食品藥品監督檢驗研究院等11家藥品檢驗機構檢驗,共17家企業生產的19批次藥品不符合規定。現將相關情況通告如下:
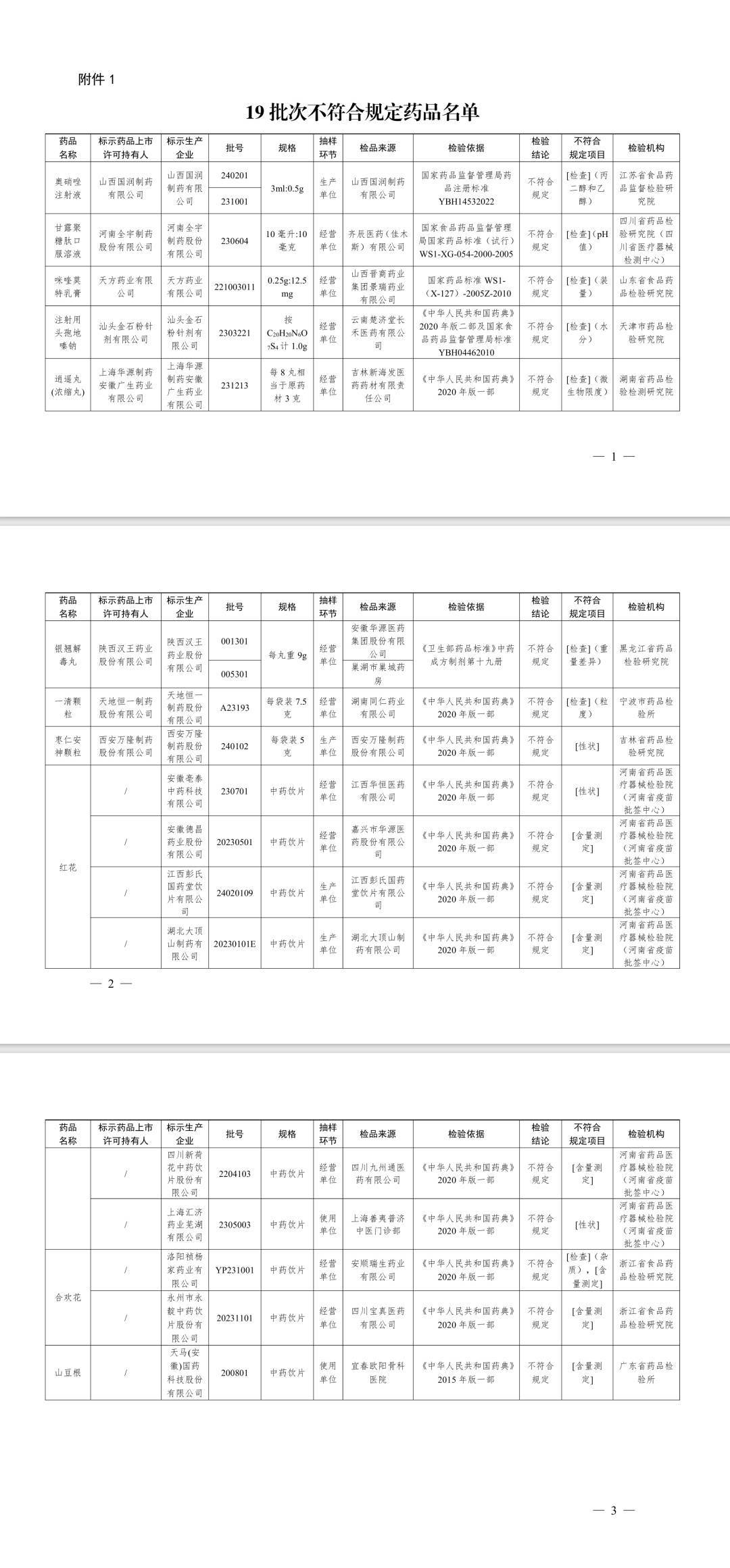
一、經江蘇省食品藥品監督檢驗研究院檢驗,標示為山西國潤製藥有限公司生產的2批次奧硝唑注射液不符合規定,不符合規定項目為丙二醇和乙醇。
經四川省藥品檢驗研究院(四川省醫療器械檢測中心)檢驗,標示為河南全宇製藥股份有限公司生產的1批次甘露聚糖肽口服溶液不符合規定,不符合規定項目為pH值。
經山東省食品藥品檢驗研究院檢驗,標示為天方藥業有限公司生產的1批次咪喹莫特乳膏不符合規定,不符合規定項目為裝量。
經天津市藥品檢驗研究院檢驗,標示為汕頭金石粉針劑有限公司生產的1批次注射用頭孢地嗪鈉不符合規定,不符合規定項目為水分。
經湖南省藥品檢驗檢測研究院檢驗,標示為上海華源製藥安徽廣生藥業有限公司生產的1批次逍遙丸(濃縮丸)不符合規定,不符合規定項目為微生物限度。
經黑龍江省藥品檢驗研究院檢驗,標示為陝西漢王藥業股份有限公司生產的2批次銀翹解毒丸不符合規定,不符合規定項目為重量差異。
經寧波市藥品檢驗所檢驗,標示為天地恆一製藥股份有限公司生產的1批次一清顆粒不符合規定,不符合規定項目為粒度。
經吉林省藥品檢驗研究院檢驗,標示為西安萬隆製藥股份有限公司生產的1批次棗仁安神顆粒不符合規定,不符合規定項目為性狀。
經河南省藥品醫療器械檢驗院(河南省疫苗批簽中心)檢驗,標示為安徽亳泰中藥科技有限公司、上海匯濟藥業蕪湖有限公司生產的2批次紅花不符合規定,不符合規定項目為性狀;標示為安徽德昌藥業股份有限公司、江西彭氏國藥堂飲片有限公司、湖北大頂山製藥有限公司、四川新荷花中藥飲片股份有限公司生產的4批次紅花不符合規定,不符合規定項目為含量測定。
經浙江省食品藥品檢驗研究院檢驗,標示為洛陽禎楊家藥業有限公司生產的1批次合歡花不符合規定,不符合規定項目為雜質、含量測定;標示為永州市永靛中藥飲片股份有限公司生產的1批次合歡花不符合規定,不符合規定項目為含量測定。
經廣東省藥品檢驗所檢驗,標示為天馬(安徽)國藥科技股份有限公司生產的1批次山豆根不符合規定,不符合規定項目為含量測定。
二、對上述不符合規定藥品,藥品監督管理部門已要求相關企業和單位採取暫停銷售使用、召回等風險控制措施,對不符合規定原因開展調查並切實進行整改。
三、國家藥品監督管理局要求相關省級藥品監督管理部門依據《中華人民共和國藥品管理法》,組織對上述企業和單位存在的涉嫌違法行為立案調查,並按規定公開查處結果。
特此通告。
附件:1.19批次不符合規定藥品名單
2.不符合規定項目的小知識
國家藥監局
2024年10月29日
19批次不符合規定藥品名單
不符合規定項目的小知識
檢查中的丙二醇和乙醇不符合規定可能影響藥物濃度。
pH值是氫離子濃度指數,作為酸鹼程度的衡量指標。
含量測定系指用規定的試驗方法測定原料及製劑中有效成分的含量,一般可採用化學、儀器或生物測定方法。水分系指藥品中的含水量。
水分偏高通常與工藝、包裝不當以及儲運環境等因素有關。
微生物限度系對非直接進入人體內環境的藥物製劑的微生物控制要求,分為計數檢查和控制菌檢查兩部分。
重量差異系反映均勻性的指標,是保證準確給藥的重要參數之一。
粒度系指顆粒的大小,不符合規定可能會導致藥物主成分含量不均一。
性狀項下記載外觀、臭、味、溶解度以及物理常數等,在一定程度上反映藥品的質量特性。中藥飲片性狀項不符合規定,可能涉及藥材種屬偏差、炮製工藝有瑕疵、儲存不當等情形。
雜質檢查系反映中藥飲片中摻入或混入雜質的情況。
綜合:國家藥品監督管理局網站、中國食品藥品監管雜誌
來源:新聞坊