受阿爾茨海默病影響的大腦中,充滿了由β澱粉樣蛋白異常聚集形成的斑塊。三十多年前,科學家們首次發現這種β澱粉樣蛋白是由澱粉樣前體蛋白(APP)產生,但一直以來人們並不清楚APP蛋白究竟有哪些神秘的生理功能。
研究人員表示,這項新發現為之前關於APP蛋白和阿爾茨海默病的研究增添了新的視角,並有望開啟全新的阿爾茨海默病治療方式。
尋找了30年的答案
20世紀80年代後期,全球幾個研究小組首次將與阿爾茨海默病密切相關的澱粉樣蛋白片段追溯到21號染色體上的APP基因。APP基因編碼出較長的蛋白質,並切割成多個片段,其中一個片段最終形成了澱粉樣蛋白斑塊。
數十年來科學家的研究集中於導致β澱粉樣蛋白片段形成及其隨後聚集的過程,以期尋找阿爾茨海默病的新治療途徑。然而距離APP蛋白首次被鑑定以來已經過去了30多年,一個重要的問題仍然沒有答案:APP蛋白的這些片段究竟發揮著什麼樣的生理功能?
為了回答這個問題,弗蘭德斯生物技術研究所大腦與疾病研究中心的BartDeStrooper和HeatherRice博士嘗試尋找與APP蛋白相互作用的神經細胞受體。
「我們知道APP蛋白通過細胞外部釋放的蛋白質發揮其作用。為了了解其功能,我們需要尋找位於細胞表面的結合受體。」HeatherRice解釋說。
最終,研究人員發現突觸(即兩個不同神經元連接傳遞信號的結構)中存在一種受體。「我們發現分泌到細胞外的部分APP蛋白,與一種名為GABABR1a的受體相互作用,並對突觸中的神經元信號傳導產生抑制。」HeatherRice說。
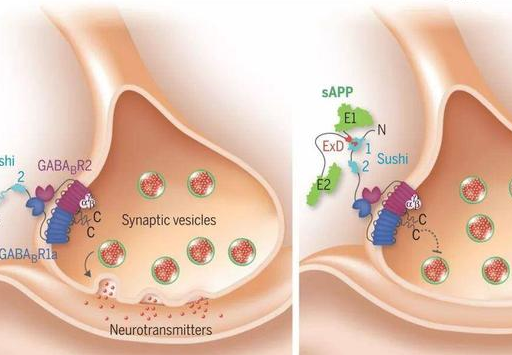
圖|分泌到細胞外的APP蛋白與受體GABABR1a相互作用(來源:Science)
「雖然阿爾茨海默病病例中APP基因的突變都會影響β澱粉樣蛋白的產生,但我們並不知道蛋白質功能的其它方面是否也會影響阿爾茨海默病。」BartDeStrooper說。
BartDeStrooper認為,這項新發現為之前關於澱粉樣前體蛋白和阿爾茨海默病的研究增添了新的視角。「新發現的APP蛋白的生理功能可能是我們在阿爾茨海默病小鼠模型和人類患者臨床發病前所見的神經網絡異常的基礎。令人興奮的是,針對這種受體的療法可能會減輕老年痴呆等疾病患者的異常症狀。」
蒙著眼睛開槍的藥物研發
在今天,人們仍然沒有找到阿爾茨海默病的確切病因,過去20年來,基於「β澱粉樣蛋白」和「tau蛋白」假說所開展的新藥研發也幾乎全軍覆沒。
因此對於阿爾茨海默病的藥物研發也被形象地比喻為「蒙著眼睛開槍」。
(圖源:麻省理工科技評論)
由於阿爾茨海默病病因不清,自2000年以來,僅美國聯邦政府對其投入的總經費已達111億美金,涉及989個機構的34649個項目。更有全球藥企巨頭數十億美元投入,十多年努力的多個藥物,均在III期臨床慘遭失敗,無疑為阿爾茨海默病的新藥研發矇上了厚厚的陰雲。
如何解開阿爾茨海默病的神秘面紗,已經成為當前科學家們需要重新思考的問題。
近幾年對阿爾茨海默病更多的發現,正在逐漸填補研究者們的「操作手冊」,更多的變體和突變被發現,更多的項目和臨床試驗也將展開。
人生的最後一道坎
阿爾茨海默病,俗稱老年痴呆症,是一種發病進程緩慢、隨著時間不斷惡化的持續性神經功能障礙。
自從1906年,德國精神病學家和病理學家愛羅斯·阿爾茨海默首次發現並以他的名字命名這種疾病至今,百餘年已經過去,人們仍舊沒有成功揭開這種疾病的神秘面紗。
與健康人相比,阿爾茲海默病患者會出現腦萎縮。在顯微鏡下,阿爾茨海默病病患大腦中的β澱粉樣斑塊和神經纖維纏結清晰可見,其中神經纖維結是由微管相關蛋白質Tau蛋白質過度磷酸化並且堆積在細胞內聚集而成。
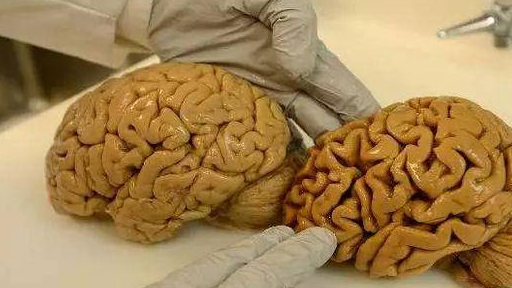
圖|阿爾茨海默病患者大腦與正常大腦對比(來源:brainrepair.ca)
這種多發於65歲以上老年人的神經系統退行性疾病,隨著年齡增大風險大幅增加,85歲以上的人群中患病風險約為50%。而且一般來說,確診後的平均存活時間僅為3-9年。
因此,阿爾茨海默病也被稱為上帝對人類最惡毒的詛咒。